Reacciones Químicas
Una gran forma de pensar en reacciones químicas es el proceso para hornear galletas. Mezcla todos los ingredientes (harina, mantequilla, sal, azúcar y huevos), y después de que la mezcla se hornea, ésta pasa a ser comida (galletas).
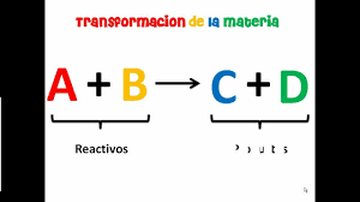
En términos químicos: la ecuación es la receta, los ingredientes son los “reactivos” y las galletas son el “producto”.
Todas las ecuaciones químicas lucen algo así “A + B --> C (+ D..)”
en donde cada letra es un elemento o una molécula (una colección de átomos unidos por enlaces químicos). La flecha representa la reacción o el cambio que ocurre.
¿Qué es una reacción química?
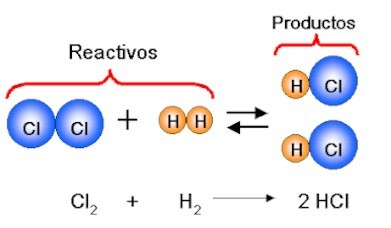
Una reacción química es un proceso por el cual una o más sustancias, llamadas reactivos,se transforman en otra u otras sustancias con propiedades diferentes, llamadas productos.
Se produce cuando dos o más sustancias se combinan transformando su composición.
La operación química mediante la cual los reactivos se transforman en productos se expresa a través de ecuaciones químicas: las sustancias se transcriben con fórmulas químicas que aluden al nombre de los átomos que las componen y se registra el sentido de la transformación.
Características de las reacciones químicas.
• La o las sustancias nuevas que se forman son diferentes a las que tenían las sustancias del comienzo.
• Durante las reacciones se desprenden o absorben energía:
- Reacción exotérmica: Ocurre cuando se desprende energía en el curso de la reacción.
- Reacción endotérmica: Ocurre cuando se absorbe energía durante el curso de la reacción.
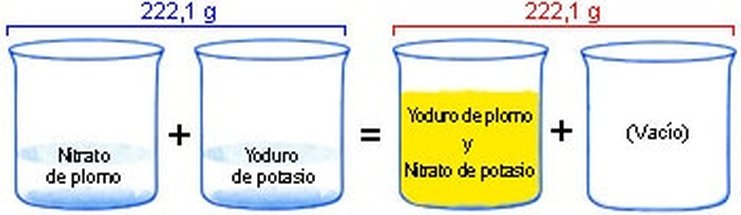
Ley de Conservación de la Masa
Si tuviéramos que decidir cuál es la ley o principio más importante en el campo de la Química no cabría ninguna duda:
El principio de conservación de la masa o ley de Lavoisier.
Esta marcó el nacimiento de la química moderna y por ello a su autor, el francés Antoine-Laurent Lavoisier ( 1743-1794), se le conoce como el padre de la química.
Se puede enunciar de distintas formas:
* La materia ni se crea ni se destruye, sólo se transforma.
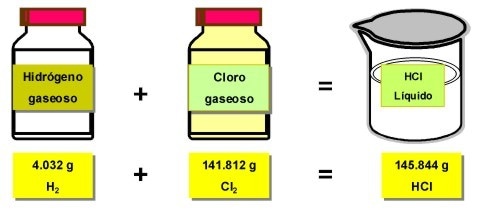
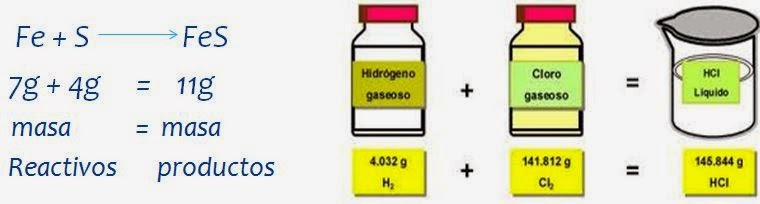
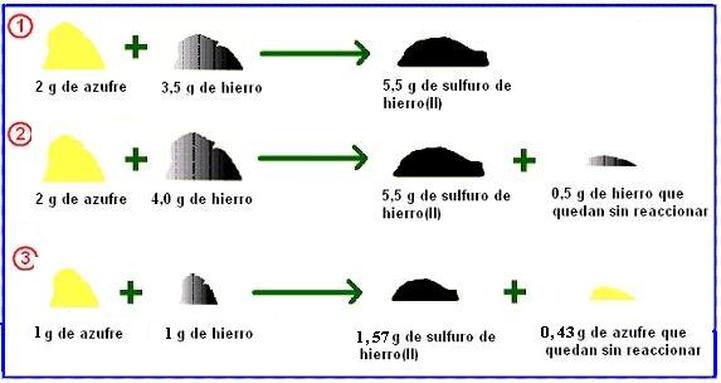
* En una reacción química la suma de la masa de los reactivos es igual a la suma de la masa de los productos.
* En una reacción química los átomos no desaparecen, simplemente se ordenan de otra manera.
Aunque te pueda parecer muy lógica y sensata esta idea, y que no tiene mucho mérito haber llegado a esa conclusión, Lavoisier tuvo que realizar numerosos y meticulosos experimentos para convencer a los que por entonces pensaban que al calentar un metal éste ganaba masa cuando se convertía en una nueva sustancia.
Lavoisier midió en un recipiente cerrado las masas del sólido y el aire antes y después de la combustión y llegó a la conclusión de que la masa que ganaba el metal era igual a la masa de aire que se perdía.
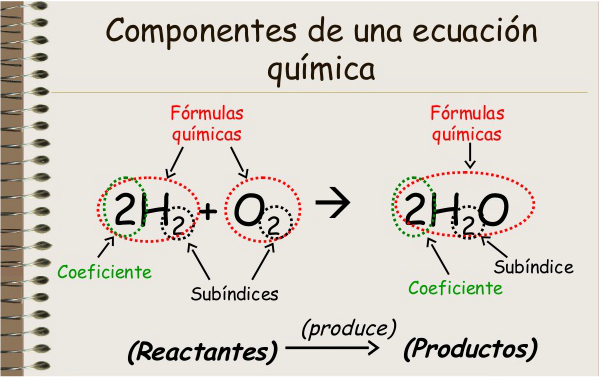
Formas de representación de una reacción química
Las reacciones químicas se representan mediante ecuaciones, las cuales siguen las siguientes reglas:
REACTIVOS ------------- PRODUCTOS
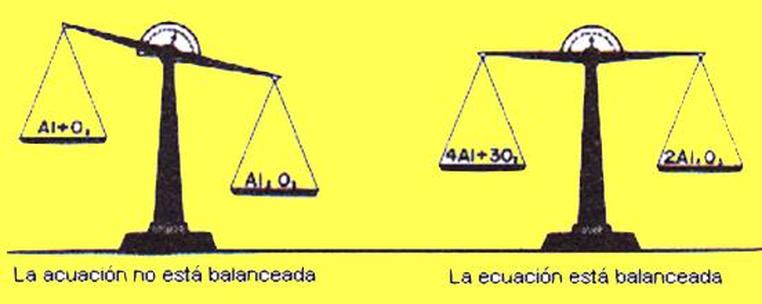
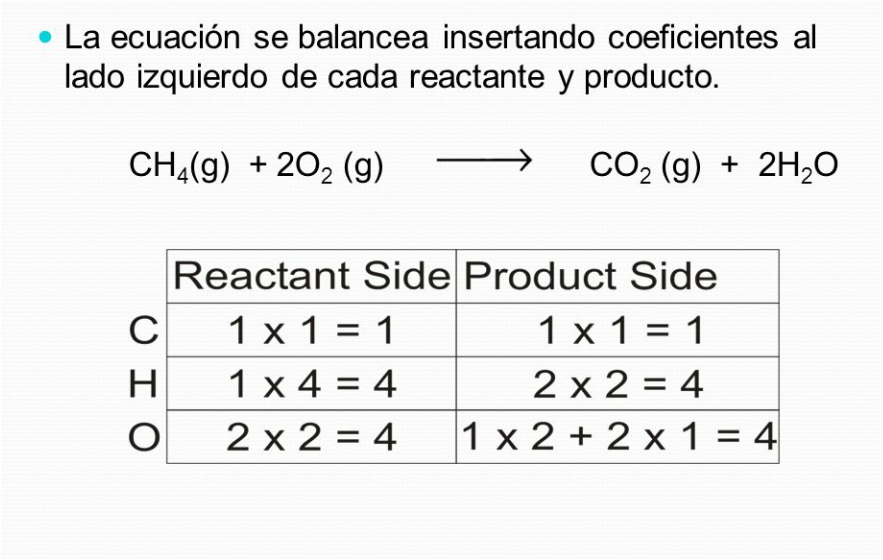
Esto nos indica que a derecha y a izquierda de la flecha, debe existir el mismo número de átomos de cada elemento.
Cuando una ecuación química cumple esta segunda regla, se dice que está ajustada o equilibrada.
Cuando las reacciones están desequilibradas (no tienen el mismo número de átomos de cada elemento), se indican delante de las fórmulas unos números llamados coeficientes, que indican el número relativo de átomos y moléculas que intervienen en la reacción.
Estos coeficientes son los únicos números en la ecuación que se pueden cambiar, mientras que los números que aparecen dentro de las fórmulas permanecen intactos, debido a que un cambio en ellos provoca un cambio de sustancia que reacciona y, por tanto, provoca una reacción distinta.
Si se quiere indicar el estado en que se encuentran las sustancias que intervienen o si se encuentran en disolución, se añaden símbolos detrás de la fórmula química correspondiente, como por ejemplo:
(s) = sólido
(l) = liquido
(g) = gas
(ac) = acuoso, disuelto en agua
Como escribir reacciones químicas?
Reacciones Químicas Equilibradas
Práctica de ejercicios de balanceo de Reacciones Químicas
| practicareacciones_químicas.pdf | |
| File Size: | 333 kb |
| File Type: | |
Clasificación de las Reacciones Químicas
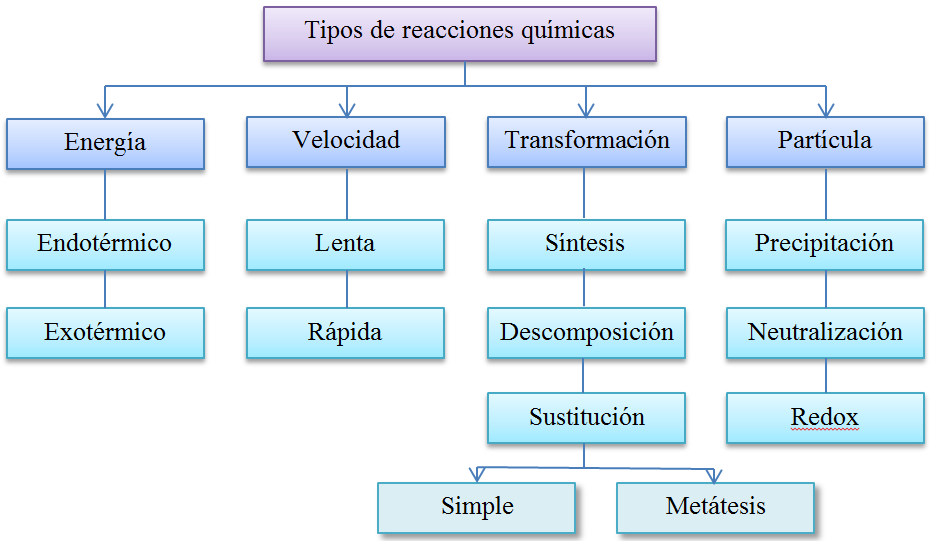
Esta sección estaremos discutiendo sobre los tipos de reacciones químicas de:
Transformación
* Síntesis
* Descomposición
* Desplazamiento simple
* Desplazamiento doble
Energía
*Endotérmica
* Exotérmica
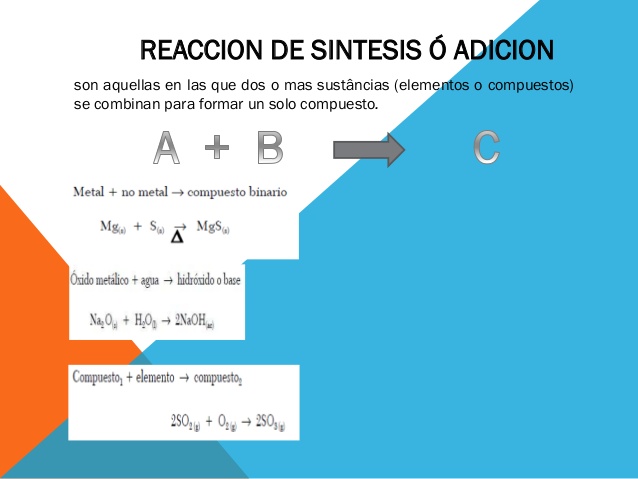
Combinación o síntesis:
Se presentan cuando se unen dos o más sustancias para formar otra sustancia, cuyas moléculas son el resultado de una reagrupación de átomos de los reactivos.
A + B → AB
Un ejemplo de esta reacción es la combinación de hidrógeno con oxígeno para producir agua:
2H2 + O2 → 2H2O
Descomposición:
Ocurre cuando a partir de un compuesto se producen dos o más sustancias.
AB → A + B
Como ejemplo tomamos al carbonato de calcio que se descompone por medio de calentamiento para producir oxido de calcio y dióxido de carbono.
CaCO3 → CaO + CO2
Desplazamiento o sustitución:
En estas reacciones, un elemento sustituye y libera a otro elemento presente en el compuesto.
En este tipo se da que:
A + BC → AC + B
Ejemplo:
El bromo líquido, que desplaza al yodo en el yoduro de sodio para producir bromuro de sodio dejando al yodo libre.
2NaI + Br2 → 2NaBr + I2
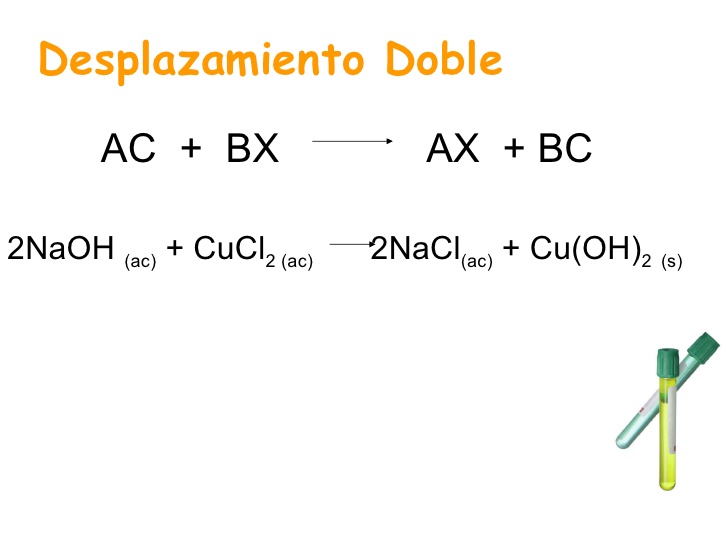
Intercambio o doble sustitución:
Al reaccionar dos compuestos estos intercambian sus elementos y se producen dos nuevos compuestos.
Se representa de esta manera:
AB + CD → AD + CB
*Ejemplo:
La combinación del ácido clorhídrico con el hidróxido de sodio y el agua.(neutralización)
HCl + NaOH → NaCl + H2O
Según el intercambio de calor o Energía:
Según el intercambio de calor existen dos clases de reacciones las exotérmicas y las endotérmicas.
Las exotérmicas presentan desprendimiento de calor.
Se denomina reacción exotérmica a cualquier reacción química que desprenda energía, ya sea como luz o como calor.
Las endotérmicas absorben el calor.
*Un ejemplo de reacción endotérmica es la producción del ozono (O3).
Esta reacción ocurre en las capas altas de la atmósfera, gracias a la radiación ultravioleta proporcionada por la energía del Sol. También se produce esta reacción en las tormentas, en las proximidades de las descargas eléctricas.
3 O2 + ENERGÍA da lugar a 2 O3
Reacción de combustión:
La combustión es una reacción química de oxidación, en la cual generalmente se desprende una gran cantidad de energía, en forma de calor y luz, manifestándose visualmente como fuego.
En toda combustión existe un elemento que arde y otro que produce la combustión, generalmente oxígeno en forma de O2 gaseoso. Los tipos más frecuentes de combustible son los materiales orgánicos que contienen carbono e hidrógeno.
Ejemplos
Práctica de ejercicios de clasificación de Reacciones Químicas
| practicaclasesrxquim..pdf | |
| File Size: | 472 kb |
| File Type: | |