Clasificación de la Materia
En este capítulo aprenderás a:
* Definir sustancias y mezclas.
* Identificar elementos y compuestos.
* Comparar y contrastar soluciones, coloides y suspensiones.
* Identificar sustancias usando propiedades físicas.
* Comparar y contrastar cambios f ísicos y químicos.
* Determinar cómo la ley de conservación de masa se aplica a los cambios químicos.
LA MATERIA Y SUS PROPIEDADES
MATERIA
*Es Todo aquello que tiene masa y ocupa un lugar en el Espacio.
* Si tiene masa y ocupa un lugar en el Espacio significa que es cuantificable, es Decir, Que Se Puede Medir.
* Todo cuanto podemos imaginar, desde un libro, un auto, la computadora y hasta la silla en que nos sentamos y el agua que bebemos, o incluso algo intangible como el aire que respiramos, está hecho de materia.
• Los planetas del Universo, los seres vivos como los insectos y los objetos inanimados como las rocas, están también hechos de materia.
CLASES DE MATERIA
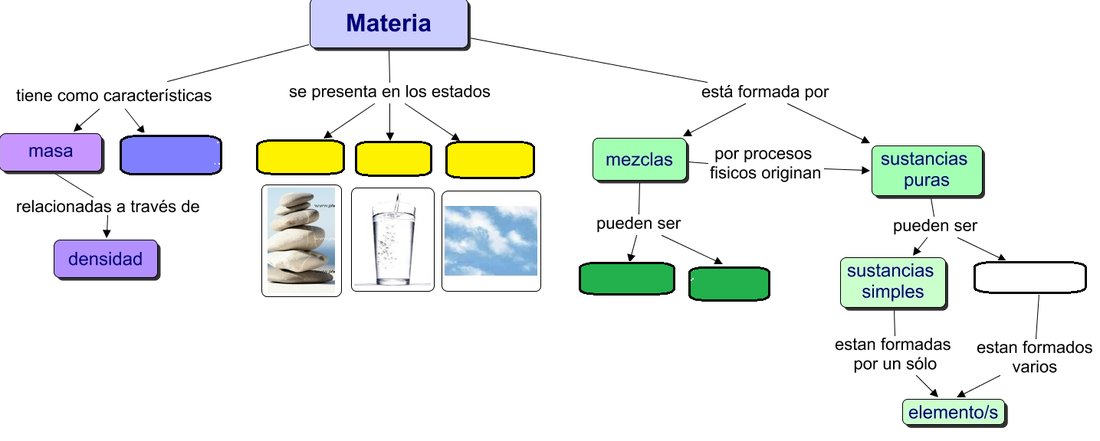
La materia puede presentarse como una sustancia pura o como una mezcla.
Sustancias Puras: Es aquella que está compuesta por un solo tipo de materia, presenta una composición fija, se clasifica en elementos y compuestos.
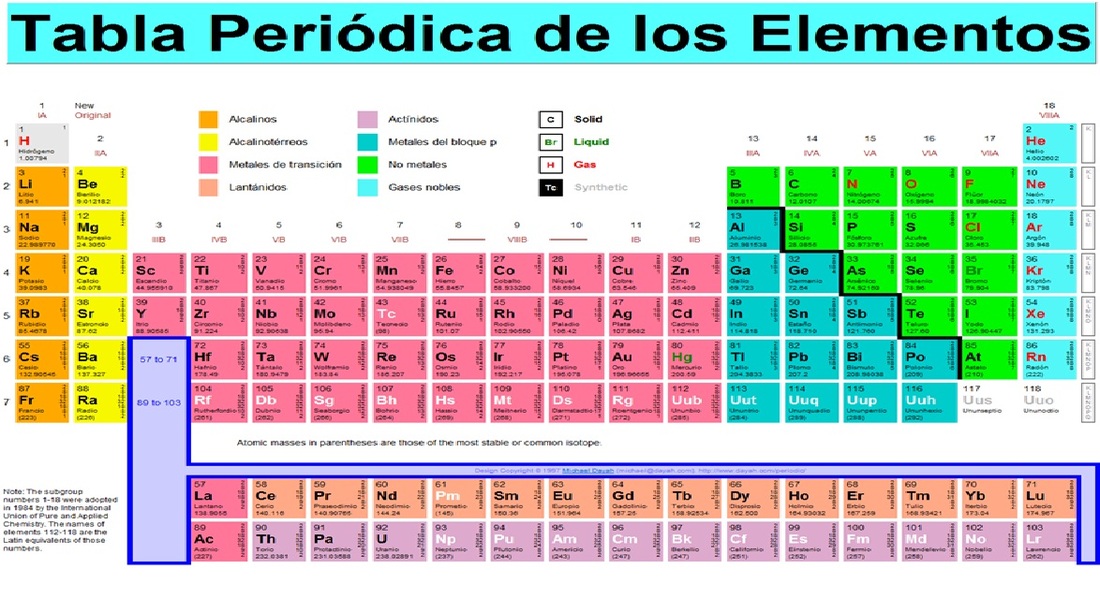
Elementos: Sustancias puras que no pueden descomponerse en otras más sencillas, se identifican mediante símbolos, clasificados en metales y no metales.
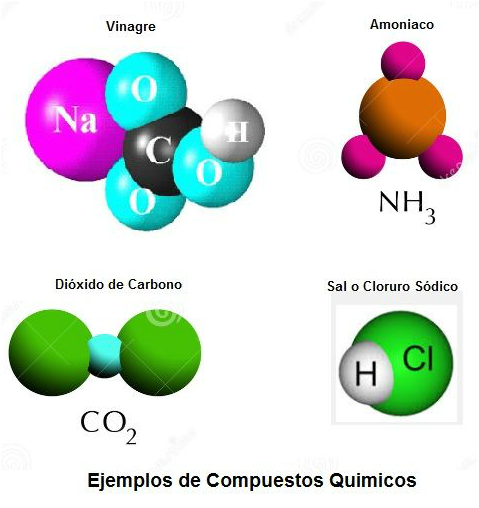
Compuestos: son sustancias formadas por la combinación química de dos o más elementos, se identifican por medio de fórmulas, donde se muestran los elementos que forman el compuesto y su proporción.
Mezclas: Son uniones físicas de sustancias donde la estructura de cada sustancia no cambia, por lo tanto sus propiedades físicas permanecen constantes, se clasifican en:
Mezclas homogéneas: son aquellas donde sus componentes no son identificables a simple vista, es decir se percibe una sola fase. También se conocen como soluciones o disoluciones.
Mezclas Heterogéneas: Son aquellas mezclas en donde sus componentes se identifican a simple vista, por ejemplo la mezcla de agua y aceite.
Dentro de las Mezclas se encuentran:
* Las Suspensiones: están formadas por un sólido en polvo o por pequeñas partículas no solubles (fase dispersa) que se dispersan en un medio líquido.
* Los Coloides : son mezclas cuyas partículas son de mayor tamaño que el de las soluciones, pero no se asientan.
Mapa Conceptual
| composición_de_la_materia.pdf | |
| File Size: | 1573 kb |
| File Type: | |
| ejemplos_de_mezclas_ejercicios_1.pdf | |
| File Size: | 285 kb |
| File Type: | |
Propiedades Físicas de la Materia
Las propiedades físicas de la materia son las propiedades que se pueden observar o medir sin cambiar la composición o identidad de la sustancia.
Ejemplos:
Color
Forma
Tamaño
Masa
Volumen
Densidad
Punto de ebullición
Punto fusión
METODOS DE SEPARACION DE MEZCLAS
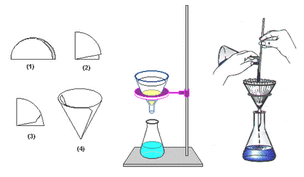
FILTRACIÓN
Este procedimiento se emplea para separar un líquido de un solido insoluble. Ejemplo: separación de agua con arena, a través de materiales porosos como papel filtro o algodón, estos materiales permiten el paso del liquido reteniendo el solido.
SEPARACIÓN MAGNÉTICA
Esta técnica sirve para separar sustancias magnéticas de otras que no lo son, al aproximar a la mezcla el imán, este atrae el material magnético separándolo del resto de la mezcla.
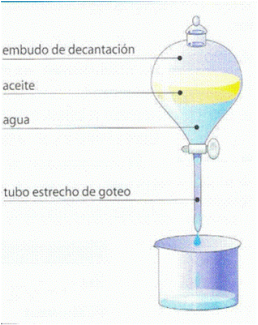
DECANTACIÓN
Se utiliza para separar dos líquidos no miscibles (que no se pueden mezclar) entre los cuales presentan distinta densidad, como por ejemplo el agua y el aceite.
Para este procedimiento se usa un embudo especial, llamado embudo de decantación. Este embudo tiene una válvula en la parte inferior. Cuando los dos líquidos están claramente separados, la válvula se abre y sale el primero, que es el líquido de mayor densidad.
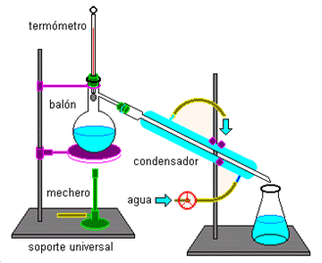
DESTILACIÓN
Proceso que consiste en separar los distintos componentes de una mezcla mediante el calor, para ello se calienta una sustancia, normalmente en estado liquido, para que sus componentes más volátiles pasen a estado gaseoso y a continuación volver esos componentes al estado líquido mediante condensación por enfriamiento.
Propiedades Físicas: Video
Propiedades Químicas de la Materia
Una propiedad química es cualquier propiedad en que la materia cambia de composición.
Cuando se enfrenta una sustancia química a distintos reactivos o condiciones experimentales puede o no reaccionar con ellos.
Las propiedades químicas se determinan por ensayos químicos y están relacionadas con la reactividad de las sustancias químicas.
Las propiedades químicas indican qué tipos de cambio pueden sufrir las sustancias.
En otras palabras, las propiedades químicas no pueden ser determinadas simplemente por ver o tocar la sustancia; la estructura interna debe ser afectada para que sus propiedades químicas sean investigadas.
Ejemplos:
Reactividad
Inflamabilidad
Corrosividad
Toxicidad
¿Cómo sabemos cuándo se ha producido una reacción química?
Cuando se produce una reacción química suelen producirse algunos indicios típicos:
Cambio de coloración: Indica la aparición de una o de varias sustancias nuevas distintas a las iniciales.
Aparición de sedimento o precipitado: Es señal de que una o algunas de las sustancias nuevas formadas son insolubles.
Desprendimiento de gas:
Como resultado de la reacción aparece una nueva sustancia que se presenta en estado gaseoso a temperatura ambiente.
Absorción o liberación de calor: Los cambios espontáneos de temperatura de la mezcla revelan que se está produciendo una reacción.
Cambios en otras propiedades: La acidez, el olor, la aparición de propiedades ópticas frente a la luz, propiedades magnéticas o eléctricas, etc.
Ejemplos de Reacciones Químicas
1. La combustión de la madera: la reduce a cenizas de carbón y libera bióxido de carbono, además de otros gases, y mientras esta reaccion se lleva a cabo se libera energía en forma de calor.
2. La unión de un átomo de oxígeno con dos de hidrógeno: produce agua
3. La corrosión que se da cuando se deja a la intemperie una estructura de hierro: ésta se oxida al entrar en contacto con el oxígeno del aire obteniéndose óxido de hierro
4. La digestión de los alimentos: cuando los seres vivos se alimentan convierten ese alimento en energía esencial para la vida.
5. La fotosíntesis: proceso mediante el cual las plantas son capaces de convertir la energía del Sol en alimento.
6. El proceso de fermentación que convierte el jugo de uva en vino: transforma los azúcares que contiene éste jugo en alcohol y gas carbónico.
7. La generación de electricidad: en una batería a partir de la energía electroquímica que se produce entre las substancias que forman la pila.
8. La respiración: mediante la cual se dan una serie de cambios químicos entre el aire y la sangre que liberan bióxido de carbono y vapor de agua a partir del oxígeno inspirado.
9. La creación de la sal: se trata del resultado de los cambios químicos producidos al combinarse el cloruro, el sodio y en ocasiones otros elementos como yodo, floruro de potasio, calcio, etc.).
Ejemplos de Reacciones Químicas en el Laboratorio: ver en el siguiente enlace la sección #2
¿Cómo se representan las reacciones químicas?
Una reacción química es un proceso en que, a partir de unas sustancias iniciales, llamadas reactivos, se obtienen unas sustancias finales distintas, llamadas productos.
Reactivos: Son las sustancias iniciales que, una vez mezcladas, reaccionan químicamente.
Productos: Son las sustancias nuevas que se forman como resultado de la reacción química entre los reactivos.
Las reacciones químicas se escriben mediante ecuaciones químicas:
a la izquierda se escriben los reactivos que se mezclan, separados por signos de sumar (+) y, a la derecha, los productos que se obtienen, separados también por signos de sumar (+).
Entre reactivos y productos se coloca una flecha, que indica el sentido de la reacción.
REACTIVOS → PRODUCTOS
Ley de Conservación de Masa
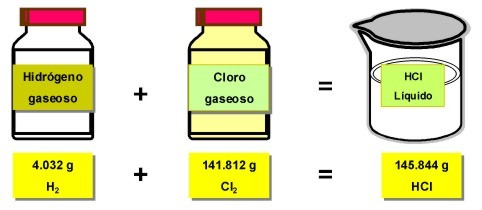
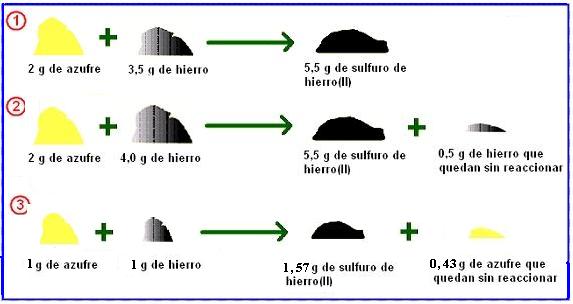
* La masa ni se crea ni se destruye.
* La masa de todas las sustancias que están presentes antes de un cambio químico equivale a la masa de todas las sustancias que quedan despues del cambio químico.
Masa Total de los REACTIVOS = Masa Total de los PRODUCTOS
Ejemplos:
| ejercicios_ley_de_conservación_masa.pdf | |
| File Size: | 11 kb |
| File Type: | |